פרוטליקס

משוך בגזר
הקמה: 1993
מיקום: פארק המדע בכרמיאל
מנכ"ל: ד"ר דוד אביעזר
מייסד: ד"ר יוסף שאלתיאל
משקיעים בולטים: ביו-סל, טכנורוב מקבוצת אלרוב, חברת הקרנות הבריטית ביילי גיפורד
פיננסים: נסחרת בתל אביב ובניו יורק לפי שווי של 2 מיליארד שקלים; גיוס הון: 144 מיליון דולרים
מועד האירוע הקובע: מאי 2012, אז תינתן תשובת ה-FDA לבקשת החברה לשיווק תרופה למחלת הגושה
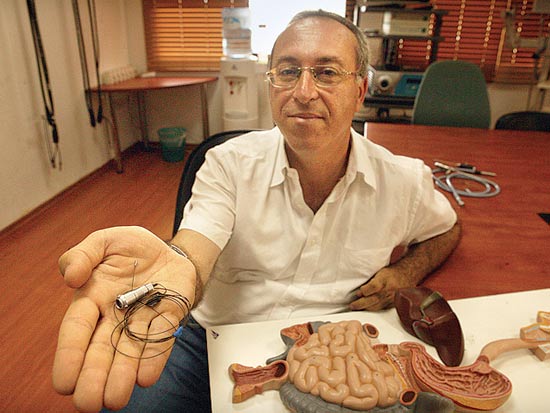
250 העובדים בפרוטליקס (Protalix) ממתינים בציפייה דרוכה ל-1 במאי. זה לא "חג הפועלים" שאליו הם נושאים עיניים, אלא לרגע שבו תודיע רשות המזון והתרופות האמריקאית (FDA) אם היא מאשרת לחברה הקטנה מכרמיאל לשווק את תרופת הדגל שלה לטיפול במחלה הגנטית הנדירה גושה. ביום הזה ייקבע אם תהפוך פרוטליקס לשחקנית ייחודית שעולה למגרש בינלאומי של ענקים, וגם לחברת הביומד הישראלית הראשונה שצלחה ב-2012 את מסלול המכשולים המפרך והמתיש של ה-FDA עד תומו.
הטכנולוגיה של פרוטליקס חלוצית בתחומה: היא מאפשרת לייצר חלבונים תרופתיים באמצעות הנדסה גנטית של תאי צמח. במקרה של התרופה לגושה, ה-Uplyso, היא עושה זאת מגזר. אם יתקבל האישור, פרוטליקס תהיה הראשונה בשוק עם תרופה ביוטכנולוגית שהופקה מתאי צמח. עד כה מוצעות תרופות ממקור של תאי חיה למחלת הגושה, שנובעת מחוסר באנזים שמפרק שומנים וגורם להצטברותם בטחול, בכבד, בכליות ובמח העצם. פרוטליקס שואפת להציע חלופה מסוכנת פחות וזולה בהרבה. אם יתקבל האישור, פרוטליקס תהפוך לשחקנית השלישית בעולם (לצד ג'נזיים האמריקאית ושייר הבריטית) המשווקת תרופה למחלה, ותנסה לנגוס בשוק שמגלגל כ-1.25 מיליארד דולרים בשנה ומיועד לכ-12 אלף חולים, שרק כמחצית מהם מטופלים כיום תרופתית - בשל העלויות הגבוהות.
השבועות הקרובים הם בבחינת סיר לחץ בחברה שמבעבע כבר כשנה וחצי, שבמהלכן חלו עיכובים שונים בדרך לקבלת אישור לשיווק התרופה. השיא היה בדצמבר האחרון, אז דחה ה-FDA את תשובתו וביקש מהחברה הבהרות נוספות - מה שהוביל את פרוטליקס למהלך של גיוס כספים ולצניחה במניה. במקביל ביקשה החברה אישור לשיווק באירופה, ועדיין לא ידוע מתי צפוי להתקבל אישור זה. אבל גם עד שיגיעו האישורים המיוחלים, במובנים רבים בשוק הביומד, פרוטליקס היא חברה שכבר עשתה את זה: ההצלחה בשלב השלישי והאחרון של הניסויים הקליניים כבר מאחוריה, והכסף הגדול, אם תינתן החותמת הנכספת, לפניה. החברה אף השלימה משימה קשה כאשר הגיעה עד לשלב המתקדם הזה בכוחות עצמה, בלי למכור את זכויות המסחור של התרופה שבדרך, בשל העלויות העצומות הכרוכות בניהול ניסויים רבי משתתפים, מנת חלקן של חברות רבות. במקום הזה עמדו עד היום רק שתי חברות ישראליות: טבע עם הקופקסון ועם האזילקט, וקמהדע עם חלבון ה-ATT. חברה אחת נוספת הביאה לשוק תרופה עצמאית, אך בינתיים רק לשוק האירופי: נעורים פארמה עם תרופת הסירקדין.
לד"ר דוד אביעזר, שמכהן כמנכ"ל פרוטליקס וכנשיאה, ברור איך הגיעה החברה עד המקום שאליו חברות ביומד מעטות מדי מגיעות: "אנחנו לא מעגלים פינות ואיננו מתביישים להיעזר ביועצים הכי טובים שאנו מצליחים למצוא, לפני שאנחנו מקבלים החלטות משמעותיות בכל תחום, כמו פיתוח, רגולציה, בניית המפעל וכדומה. אנחנו לא חושבים שאנחנו הכי חכמים בעולם ושאנחנו יודעים הכול, אלא מנסים להיעזר במאגרי ידע קיימים".
לחברה יש תוכנית פעולה מפורטת, שתצא לפועל מרגע הישמע הגונג במשרדי ה-FDA במרילנד. "אנחנו נערכים מבחינה תפעולית לסדרת פעולות לקראת תרחיש שאנחנו מעריכים שיתגשם", כך אביעזר, "החל בעיצוב האריזה והקופסה, עבור בהיערכות לוגיסטית של אספקת התרופה והשינוע שלה, וכלה בחיזוק הצוות השיווקי. ההיערכות מתבצעת תחת הובלתה של השותפה האסטרטגית שלנו פייזר. הרבה מאוד צוותים נערכים ליום שאחרי".
- כמה זמן אתם עמלים על פיתוח התרופה?
"עשר שנים. התחלנו כסטארט-אפ קטן באזור המוסכים של קריית שמונה, והיום אנו פועלים במתקן ייצור ביוטכנולוגי מן השורה הראשונה בעולם, שהקמנו בכרמיאל. תהליך ארוך ומאתגר זה יגיע, כך אנו מקווים ומאמינים, להישג משמעותי נוסף עם קבלת האישור, ובכך נעבור משוכה חשובה מאוד, שתאפשר לנו להתחיל למצות את הפוטנציאל הרב הטמון בתרופה שלנו ובפלטפורמה היחידה מסוגה בעולם שהצלחנו לפתח".
"אין תוכניות מכירה"
פרוטליקס עברה חבלי לידה לא שגרתיים. כבר בשלב מוקדם יחסית זכה הפוטנציאל שלה להבעת אמון מצד בכירים בתעשייה, ביניהם השקעות גדולות של קרן פונטיפקס בראשות היו"ר דאז אלי הורביץ, ושל פיליפ פרוסט, המכהן כיום כיושב ראש טבע. הדחיפה הבאה במעלה התלול של ההר הגיעה דווקא מהספקית הכמעט בלעדית של תרופה לגושה ומי שבקרוב עשויה להפוך למתחרה הגדולה של פרוטקליס - ג'נזיים האמריקאית. כידוע, צרות של חברה אחת הן ההזדמנות של חברה אחרת, וכך, כשג'נזיים הודיעה בשלהי 2009 על השהיית ייצור התרופה שלה בעקבות זיהום במפעל, בשוק נרשם מחסור קריטי.
כמעט במקביל הודיעה פרוטליקס על הצלחה בשלב השלישי של הניסויים, ובהליך חריג אישר לה ה-FDA לספק את התרופה לכמה עשרות חולים. היתר לא שגרתי זה סיפק לפרוטליקס הזדמנות להרחיב את מספר החולים המתנסים בתרופה, ולמעשה בפירותיה של הטכנולוגיה החדשנית מן הצומח. התרופה נרשמת כיום לכמה מאות חולים בעולם, חלקם כאלה שלא היו יכולים להשיג את התרופה של ג'נזיים בשל המחסור.
נקודת ציון משמעותית נוספת בגלגולה של פרוטליקס היא הגב החזק והמנוסה שלה בשיווק: במסגרת הסכם שחתמה ב-2009 עם פייזר, תהיה ענקית התרופות האמריקאית אחראית על השיווק בעולם (מלבד בישראל), ואילו פרוטליקס על הייצור.
- איזו אווירה שוררת בחברה בימים אלה?
אביעזר: "חשוב לי להדגיש כי לפני הכול, ההחלטה צריכה להינתן על-ידי ה-FDA. שיקוליו אינם בהכרח ידועים לנו, ולכן אין לנו ודאות לגבי מהות ההחלטה. יחד עם זאת, לדעתנו ועל-פי מיטב הערכתנו, התרופה עובדת. יש מאות חולים בעולם שטופלו בתרופה הזאת, רמת הביטחון שלנו גבוהה, ואנחנו אופטימיים. כולם מתכוננים ומחכים לאישור, ויש בחברה דריכות רבה; זה כמעט מפעל חיים של עובדים רבים בפרוטליקס".
אביעזר מסביר כי האישור ייתן הכרה לשימוש בחלבונים ביוטכנולוגיים ויהווה קרש קפיצה עבור החברה: "בטכנולוגיה הזאת נוכל לייצר גם את התרופה השנייה, העשירית וה-25. לכן לאישור יש משקל רב, הרבה מעבר לתרופה הספציפית, החשובה לכשעצמה. למרות זאת, הצלחה במוצר הראשון אינה ערובה מוחלטת לאישור המוצר השני, וגם להפך. כלומר, גם דחייה בקבלת האישור אינה בהכרח משפיעה על אישור התרופות הבאות שבפיתוח".
פרוטליקס, הפועלת בתחום של תרופות יתום, מפתחת גם תרופה לפאברי, מחלת אגירה גנטית. במקביל היא מפתחת מוצרים הקשורים למערכת העצבית, כמו הגנה נגד גז עצבים, ובודקת שימושים נוספים הקשורים למחלות במערכת העצבים, כמו אלצהיימר ופרקינסון. אביעזר אף מציין כי "אם וכאשר יתקבל אישור, הוא צפוי להגביר עשרת מונים את ההתעניינות של חברות תרופות גדולות מאוד בטכנולוגיה שלנו".
- מה לגבי מכירת החברה?
"אין לנו תוכנית כזו. אנחנו בהחלט חושבים שיש לנו עוד הרבה מאוד מה לעשות עם הפלטפורמה שלנו כדי להמשיך לייצר ערך עתידי. עם זאת, בעולם העסקי אסור להגיד 'לעולם לא'. בכל מקרה, לחברה יש תוכניות ברורות איך להתקדם ולמנף באופן אקטיבי ואגרסיבי את ההצלחה הראשונה והמיוחלת".
- איזה רגע מרגש אתה זוכר מהדרך שעשתה החברה עד כה?
"אני נמנע מליזום קשר באופן אקטיבי עם חולים, בשל שמירה על פרטיותם, אבל כשבאחד הכנסים שנערכו על מחלת הגושה ניגש אליי חולה שמטופל בתרופה שלנו, וביקש להודות לנו ותיאר כיצד מצבו הרפואי השתפר, ואיך כאבי עצמות קשים שהיו לו חלפו, והוא חזר לעסוק בפעילות גופנית - הדבר נתן לי תחושת סיפוק אדירה".
מדיגוס
הסוף לצרבת
הוקמה: 2000
מיקום: פארק התעשייה עומר
מנכ"ל: ד"ר אלעזר זוננשיין
מייסדים: אלעזר זוננשיין ואחיו מנשה (המשמש כמנהל מחקר ופיתוח), יאיר רבינוביץ' (המשמש כיו"ר), אביאל שפירא ומשפחת לוצאטו
משקיעים בולטים: דן אורן (באמצעות חברת דקסון), האחים זוננשיין, ג'ונסון אנד ג'ונסון, כפיר לוצאטו, יאיר רבינוביץ'
פיננסים: נסחרת בתל אביב לפי שווי של 58 מיליון שקלים; גיוס הון עד היום: 22.2 מיליון דולרים (על-פי נתוני IVC)
מועד האירוע הקובע: בתוך שישה עד שמונה שבועות תתקבל תשובת ה-FDA לאישור שיווק אנדוסקופ לטיפול בצרבת חריפה. באותה תקופה צפויה להתקבל תשובה גם מהרשויות בקנדה
ד"ר אלעזר זוננשיין, מנכ"ל וממייסדי חברת המכשור הרפואי מדיגוס (Medigus), יודע בדיוק מה יעשה אם בעוד פחות מחודשיים תשגר ה-FDA את התשובה החיובית הנכספת, שלה מצפה החברה כבר יותר מעשור: הוא יצא עם המשפחה לוויקאנד. "אחרי התקופה הזאת, מגיע להם", הוא אומר בחיוך.
מדיגוס עוסקת בפיתוח פרוצדורות רפואיות מבוססות אנדוסקופיה. הפיתוח המוביל שבהן הוא ה-SRS - אנדוסקופ לטיפול בצרבת חריפה (GERD), מחלה שבה השסתום שמפריד בין הוושט לקיבה אינו פועל כהלכה ולא מונע את החזרת נוזלי הקיבה לוושט. על-פי ההערכות, כ-7% מאוכלוסיית העולם סובלים מהתופעה.
מרבית החולים מקבלים טיפול תרופתי, ואם זה אינו יעיל דיו עבורם הם נאלצים לעבור ניתוח. המוצר של מדיגוס שואף להחליף את הניתוח בפרוצדורה פולשנית פחות: האנדוסקופ הגמיש מוכנס לגוף דרך הפה וכולל כוונת אולטרה-סאונד, מצלמת וידיאו זעירה ומהדק רקמות, והוא מחזק את השסתום ללא צורך בניתוח. בשנה שעברה קיבל המוצר אישור שיווק באירופה, והמוצר החל להימכר שם. עד כה חתמה מדיגוס על הסכמי הפצה בטורקיה, בספרד, ביוון ובקפריסין, וכן על מזכר הבנות להסכם הפצה בהודו.
ההתחלה הייתה יומרנית: זוננשיין הגיע אל יאיר רבינוביץ', היום יו"ר החברה, עם רעיון בוסרי. רבינוביץ' תפס אותו בשתי ידיים וכבר באותו ערב החל לגייס כספים. הסטארט-אפ הצעיר שהוקם כלל קומץ משוגעים לדבר, שלא הבינו הרבה בתחום האנדוסקופיה ושאפו להתחרות בשועלים ותיקים ומנוסים בשוק. עשר שנים אחרי, הרעיון הבשיל למוצר. "באתי עם גרעין, ומשם הוא קיבל כיוונים שונים והתפתח מאוד; אני לא יכול לקחת את כל הקרדיט לעצמי", אומר זוננשיין.
- איך הרגשת כשקיבלת את תוצאות הניסויים האחרונים, השלב השלישי?
"התוצאות הגיעו במייל לפני שלושה חודשים, קצת לפני כניסת שבת. זה היה רגע של אושר. היו לנו נתונים גולמיים, וכבר מהם עלה שאנחנו בסדר, אבל צריך את האישור הסופי".
- איזו אווירה שוררת במסדרונות החברה?
"אנחנו מצפים לקבל את האישור ועושים את כל ההכנות, כמו היערכות להגדלת קצב הייצור. העשייה רבה; חתמנו על עסקות עם כמה מדינות, וזה דורש מאיתנו לספק את הביקוש, ואני מאמין שבשבועות הקרובים נשמע על חוזים נוספים. האישור מארצות הברית יהיה בשבילנו הישג נוסף ואבן דרך חשובה בחיי החברה".
- חשבת מה תעשה אם לא תקבלו את האישור?
"אני לא סבור שלא נקבל אישור. יכול להיות שנתבקש להעביר הסברים נוספים, וזה לגיטימי. אנחנו יודעים שבמבחנים של בטיחות ושל יעילות - עמדנו".
- אילו שווקים תפתח בפניכם החותמת של ה-FDA?
"ארצות הברית היא שוק חשוב מאוד: המעגל הראשון שם כולל מטופלים שלא מגיבים היטב לתרופות וחוששים מניתוחים, והשוק הזה מוערך ב-8.5 מיליארד דולרים. המעגל השני כולל חולים שנמצאים על מינון כפול או משולש, אינם שבעי רצון מהטיפול, ומחפשים פתרון לעונש של התרופות - מעגל שנאמד ב-10 מיליארד דולרים נוספים. כלומר, יש לנו הרבה עבודה לעשרים השנים הקרובות".
- למה לדעתך חברות ביומד ישראליות מעטות מגיעות לשלב הזה?
"בגלל חוסר בהשקעות גדולות. כמה חברות ביומד ציבוריות יש בישראל שהושקעו בהן 100 מיליון דולרים? מעט מאוד. בארצות הברית, אין מצב שהשקיעו בחברה פחות מ-60-70 מיליון. חוסר ההשקעות גורם לתהליכים להיות ארוכים יותר, ומאיתנו הוא דורש להיות יצירתיים ולחשוב איך עושים את כל התהליך נכון, במינימום כסף וטעויות".
כן פייט ביופרמה

נותנת פייט
הוקמה: 2000
מיקום: פתח תקוה
מנכ"לית: פרופ' פנינה פישמן
מייסדים: פרופ' פישמן וד"ר אילן כהן
משקיעים בולטים: טל שקד, דנאלי ונצ'רס, אסנד טכנולוגיות, גיזה
פיננסים: נסחרת בתל אביב לפי שווי של כ-99 מיליון שקלים; גיוס הון: כ-35 מיליון דולרים (על-פי נתוני IVC)
מועד האירוע הקובע: במחצית השנייה של השנה מחכה החברה לתוצאות שלבי IIB בתרופות לפסוריאזיס ולדלקת מפרקים
פרופ' פנינה פישמן מלווה את התרופה CF-101 עוד מהימים שבהם המטרה שאותה תוקפת התרופה התגלתה לה בצלחת פטרי באקדמיה. "הייתי חוקרת אקדמית במרכז הרפואי רבין, ושם מצאנו כי תאים החולים בסרטן מאופיינים בקולטן מסוים, ואילו תאים בריאים אינם מבטאים אותו. ברגע שראיתי את זה, כבר הייתה לי ראייה לטווח רחוק. ידעתי שההבדל הזה יכול להוביל לפיתוח תרופה, וגם הבנתי שבמסגרת האקדמיה יהיה קשה להשיג את המשאבים. ידעתי שכדי לקדם את המוצר נהיה חייבים להקים חברה מסחרית".
פישמן הקימה את כן פייט ביופרמה ב-2000, ומאז היא מזוהה עם החברה. "התחלתי בלי לדעת כמה רחוק אלך עם החברה, אבל אמרתי לעצמי שאם אני לא אתחיל את זה - זה לא יקרה. מיד עם הקמת החברה שכרתי שני מומחים, סגן נשיא לפיתוח ומנהל רפואי, ששניהם הגיעו מן התעשייה והאירו לנו את הדרך לפיתוח המוצר, כמו עם פנס".
- הייתם בעבר רגע לפני הכרעה, כשהמוצר שלכם לדלקת מפרקים נכשל בשלב IIB של הניסויים.
"בחברת ביוטק אתה תמיד לפני הכרעה. גם בשלב הבטיחות, שמושך פחות תשומת לב חיצונית, נופלים 95% מהתרופות. לנו באמת הייתה ב-2009 שנה קשה, כשהמוצר שלנו לדלקת מפרקים נכשל בניסוי שבו בחנו אותו בשילוב עם התרופה מטוטרוקסט. זה קרה ביום העצמאות דווקא, ואני הייתי בארצות הברית. הלכנו להיפגש עם הצוות הסטטיסטי, ומה אגיד - אני לא אשכח לעולם את הרגע הזה. אתה מרגיש שהעולם נגמר לך, שאתה הולך למות".
- איך מתאוששים?
"במקרה שלנו, נאחזנו בעובדות המדעיות ובנתונים, ומה שהנתונים הראו הוא שאצל אוכלוסיית החולים שנבדקה, לרובם לא היה על התאים החולים את הקולטן שזוהה אצלי עוד במעבדת המחקר בבית החולים.
"כמו כן ידענו שבניסוי קודם שעשינו, כשהשתמשנו במוצר שלנו כתרופה יחידה, כן הייתה תועלת, אולם ה-FDA דרשה באותו הזמן לבצע כל ניסוי במוצר לדלקת מפרקים בשילוב עם מטוטרוקסט, ואנחנו הבנו עם הזמן שהשילוב הזה הוא לא טוב. די מהר התעשתנו, והבנו שאנחנו צריכים לחזור על הניסוי שוב, תוך ברירת החולים שישנו אצלם הקולטן, ולא בשילוב עם תרופה נוספת. זה מה שאנחנו עושים עכשיו".
- איך את מתמודדת עם זה שדווקא בשלב ההכרעה אין לך שליטה על המתרחש?
"בן האדם הוא החיה הכי סתגלנית בטבע. זו אחת ההגדרות של נורמליות, להסתגל. לכן בן אדם מסתגל לחיות גם במצבי לחץ, עסוק בעשייה אחרת, ולא חושב כל היום מה יהיה. השילוב הזה בין העשייה לבין הציפייה מהווה מנוע שכל הזמן דוחף הלאה. לשמחתי, הסל שלנו מאוד מגוון כיום מבחינת סוגי הניסויים שאנחנו עושים, ולאור תוצאות שקיבלנו בעבר, אנחנו חיים כיום בתחושה שחלק מהדברים ודאי יצליח".
- המשפחה מעורבת בתהליך? הם יודעים, למשל, מתי התוצאות יתקבלו?
"המשפחה לא יודעת את התאריך המדויק כי זה חסוי, ובאופן כללי אני פחות מערבת את המשפחה בפרטי-הפרטים, כי ההפרדה בין הזירות היא חשובה לבריאותה נפשית".
- מתקשרים משקיעים, אנליסטים?
"כן, אבל זה דווקא קל להגיד שאני לא יודעת. כי באמת אנחנו לא יודעים כלום על התוצאות".
- גם כשהתוצאות היו פחות טובות, אנשים צלצלו? משקיעים כעסו?
"בטח, כשהיו תוצאות לא טובות כולם התקשרו לדרוש הסבר. במצבים קשים אתה מקבל כוחות שאתה בכלל לא יודע מאיפה אתה מביא אותם. יש מערכת של הורמונים שאחראית להביא לך את הכוחות הללו, והיא פועלת לשמחתי גם בכיוון השני - היום שבו ניסוי מצליח הוא יום מדהים, והוא נותן כוחות להמשיך דרך ארוכה הלאה".
- איך את מדמיינת את היום של ההצלחה?
"אני עסוקה ביומיום ולא מפנטזת על ההצלחה, אבל יש אופק של טיפול בחולים, והדלק בא בעיקר משם. כבר כיום יש חולים שמטופלים בתרופות שלנו - זה ממלא באושר ובציפייה חיובית".
בריינסוויי
הוקמה: 2003
מיקום: הר חוצבים, ירושלים
מנכ"ל: עוזי סופר
מייסדים: פרופ' אברהם (בומי) צנגן, ד"ר יפתח רוט, עוזי סופר, ד"ר דוד זכות וחגי אבנר. הם גם המשקיעים העיקריים
פיננסים: נסחרת בתל אביב לפי שווי של כ-200 מיליון שקלים; גיוס הון: כ-10 מיליון דולרים (על-פי נתוני IVC)
מועד האירוע הקובע: אפריל הקרוב, אז צפויה החברה לקבל את תוצאות השלב האחרון של הניסויים בטיפול בדיכאון מז'ורי בטכנולוגיית DTMS שפיתחה
חברת המכשור הרפואי בריינסוויי (Brainsway) אינה צועדת בשבילים המקובלים בענף הביומד. היא אינה מתמקדת בפיתוח מוצר למחלה אחת או שתיים, אלא חולמת על תעשייה שלמה, שיום אחד אולי תצליח לתת מענה למגוון של מחלות. "אני חושב שכדי להצליח בצורה יוצאת דופן, צריך להיות שונים. אם הולכים בפלטפורמה סטנדרטית, לא תהיה איזו הצלחה מטאורית", אמר המנכ"ל עוזי סופר בראיון מקיף ל-G בדצמבר האחרון.
בריינסוויי, שמעסיקה ארבעים עובדים, מפתחת מכשיר דמוי קסדה, המבוסס על טכנולוגיה לא פולשנית לטיפול באמצעות גירוי מגנטי מוחי, המכונה TMS (Transcranial Magnetic Stimulation). כשהגירוי הזה מכוון לאזורים שונים במוח הוא עשוי - על-פי מיקומו - לעורר או לדכא פעילות עצבית, ובכך לטפל במחלות פסיכיאטריות ונירולוגיות.
הטיפול ב-TMS פותח ב-1985, ומאז 2008 אושר לשימוש על-ידי ה-FDA. החידוש של בריינסוויי הוא בכך שבעוד שה-TMS מגרה את קליפת המוח בעומק של 1.5 עד שני סנטימטרים בלבד, הטכנולוגיה של החברה מאפשרת לחדור לעומק של שישה-שבעה סנטימטרים (Deep TMS); כלומר לאזורים הרלבנטיים בתחומי הדיכאון וההתמכרות, במקום לגרות את כל המוח.
לבריינסוויי יש אישור לשווק באירופה את המכשיר לטיפול בלוקים בדיכאון, במאניה-דפרסיה ובהפרעת דחק פוסט טראומטית. החברה מעריכה כי עד תום 2012 יחל שיווק המכשיר גם בדרום אמריקה. לפני חודשים ספורים היא רשמה לעצמה נקודת ציון נוספת, כשקיבלה אישור ממשרד הבריאות לשווק בישראל את המכשיר לטיפול בדיכאון, במאניה-דפרסיה ובסכיזופרניה לכמה מרכזים רפואיים בארץ.
באפריל הקרוב יתקבלו תוצאות ראשוניות מהשלב האחרון של הניסויים בטיפול בדיכאון - תוצאות ניסוי רב מרכזי Multi Center)). "אנחנו מתפללים שהדברים יהיו טובים", כך סופר השבוע. "יש התרגשות ומתיחות בחברה, אבל יש לנו עוד הרבה אינדיקציות שאנחנו מפתחים. במקביל אנחנו עובדים על השוק באירופה ובדרום אמריקה ועסוקים במעבר מפיתוח לייצור".
אם התוצאות יהיו טובות, החברה תגיש בקשה לשיווק ל-FDA כמה חודשים אחר כך, כלומר לקראת סוף 2012. "ב-FDA לא תמיד התוצאות הן בינאריות", מזכיר סופר. "יכול להיות שהרשות תדרוש מידע נוסף, או שיהיו תוצאות חלקיות. אנחנו נערכים גם אם חלילה יהיה תרחיש רע, ומקווים לתוצאות טובות".
אפוסנס
זמן אמת
הוקמה: 1996
מיקום: פתח תקוה
מנכ"ל: יורם אשרי
מייסד: ד"ר אילן זיו
משקיעים בולטים: ברגל השקעות (בשליטת יעקב גוטנשטיין ואלכס פסל), אילן זיו, הרטווד, מורי בלומנפלד, קרנות פנסיה ותיקות והפניקס
פיננסים: נסחרת בתל אביב לפי שווי של 280 מיליון שקלים; גיוס הון: 67 מיליון דולרים (נתוני IVC)
מועד אירוע קובע: ספטמבר-אוקטובר, אז יתקבלו תוצאות השלב השני והמכריע של הניסויים הקליניים במערכת המאבחנת את מידת השפעתם של טיפולי סרטן על החולה
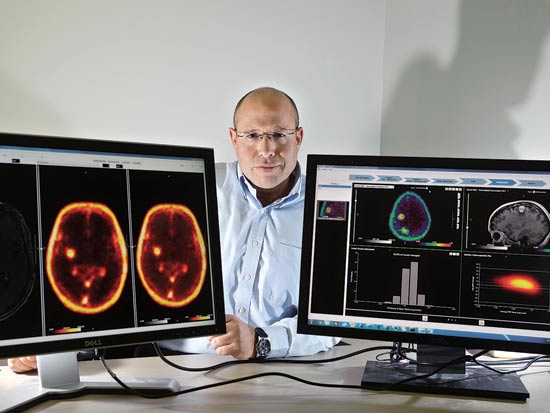
דמיינו את התרחיש החדשני הבא: חולה סרטן עובר כימותרפיה או הקרנות, ואחרי שעות ספורות בלבד מקבל תשובה אם הטיפולים שעבר משפיעים באופן אפקטיבי על הגידול שבגופו (כיום ניתן לנפק תשובה כזאת רק לאחר טיפול בן חודשיים או שלושה, באמצעות הדמיות ב-CT או ב-MRI). את השאיפה היומרנית הזאת מובילה אפוסנס (Aposense) מפתח תקוה. החברה עוסקת בפיתוח מוצרי הדמיה מולקולרית ותרופות שמבוססים על טכנולוגיה ייחודית שלה, המאפשרת לזהות בגוף תאים הנמצאים בתהליך של "מוות מבוקר" (אפופטוזיס או "התאבדות" של תאים).
מוצר ההדמיה המתקדם ביותר מבחינת פיתוח הוא מערכת דיאגנוסטיקה בשם EarliTest, המאפשרת למפות בשלב מוקדם של מחלת הסרטן את מותם של תאים, ולבדוק בזמן אמת את יעילות טיפולי הכימותרפיה וסוגי ההקרנות השונים. הדבר מתבצע באמצעות סמן מולקולרי: מוצר שפיתחה החברה, שמוזרק לגוף ונקשר לתאים שעוברים אפופטוזיס.
במקרה של אפוסנס ושלושים עובדיה, ה-FDA נמצא באופק הרחוק יותר - אי-שם במהלך 2014. אולם השנה הנוכחית תקבע במובנים רבים את עתידה של החברה: תוצאות השלב השני של הניסויים הקליניים צפויות להתקבל במחצית השנייה של 2012, והן השלב המכריע ביותר עם הסיכון הרב ביותר, שאחריו יתברר אם המוצר יעיל. מדובר באחד המחקרים הבינלאומיים הגדולים ביותר בתחום הסרטן שעורכת חברה מישראל, והם מתבצעים ב-16 מרכזים רפואיים. "ההצלחה של הניסויים הנוכחיים תקבע את עתיד החברה", מאשר המנכ"ל יורם אשרי. אם יתקבלו תוצאות טובות, תזנק החברה לשלב השלישי והאחרון של הניסויים, ומשם - לזרועות ה-FDA. "היכולת להתביית על תאים מתים ולבחון אותם זו יכולת ייחודית שפיתחנו. לא היינו הראשונים שניסינו, אבל אנחנו היחידים שהצלחנו".
את פוטנציאל השוק של המוצר מעריך אשרי ב"מיליארד דולרים בשנה וצפונה", בהנחה שמדי שנה ישנם 1.3 מיליון חולים שיכולים לעבור את ההדמיה מבחינה פיזיולוגית.
- ומה עכשיו, כוססים ציפורניים?
"כמו לקראת עלייה לתורה בבר מצווה", צוחק אשרי. "בתפקידי הקודם שימשתי כסמנכ"ל פיתוח עסקי בחברת גיוון אימג'ינג, והמתנה היפה ביותר שקיבלתי היא ללוות מוצר משלב הרעיון למשהו גשמי; המחשבה שיום אחד מישהו יבלע את אותה קפסולה וזה יעזור לו לאבחון, זאת חוויה שקשה לתאר ויש בה סיפוק עצום. השנה אדע אם אחווה את החוויה הזאת שוב. אני אופטימי מטבעי, ואני מקווה שנצליח. כל עובדי החברה רתומים לעניין ומאמינים בו".
אפוסנס יצאה לפני כשנתיים להנפקה בשווי גבוה מאוד יחסית למקובל בענף, בין היתר בזכות תמיכתו של אלי הורביץ ז"ל, שאף כיהן כיו"ר החברה. מאז נחתכה מנייתה ביותר מחצי, והמשקיעים הנוכחיים ממתינים כבר זמן רב לבשורה מניסויי הדיאגנוסטיקה - ולהספקת הסחורה. "פיתוח קליני בשלב 2 אינו מיועד לאנשים עם לב חלש", מבהירה ד"ר מירי בן-עמי, סמנכ"לית הפיתוח בחברה. "תכנון ארוך ומעמיק של המחקר הקליני זה מאמץ גדול, שבצדו קצת רעד והמון התרגשות. מרוב המאמץ העבודה אין יותר מדי זמן לחשוב על הצד המפחיד".
בן-עמי, לשעבר בכירה בטבע, עזבה את מקצועה כגינקולוגית לטובת עולם פיתוח התרופות. "אני לא יכולה לחכות לחוות את תחושת הסיפוק מההצלחה להביא תרופה משלב מוקדם במעבדה אל החולים. עזבתי את עולם הרפואה בגלל פוטנציאל ההשפעה על מאות אלפי אנשים. זה החלום".
- חשבתם מה תעשו אם הניסוי לא יצליח?
אשרי: "אנחנו לא חברה בינארית, אנחנו רצים בכמה מישורים במקביל, ובתחום ההדמיה יש לנו כמה מוצרים (לחברה יש הסכם עם טבע, שבמסגרתו הן מפתחות יחד תרופות לטיפול בסרטן, שעוברות הנחיה ממוקדת באמצעות מולקולות של אפוסנס). כולם יושבים על אותה פלטפורמה לזיהוי תאים מתים, והיא מוכחת חד-משמעית. הסיכון הוא כשמלבישים עליה כלים חדשים. עם האפסייד נתמודד מצוין, עם הדאונסייד נתמודד כל הזמן, ולכן חלק חשוב מאוד בעבודה שלנו הוא ניהול סיכונים מוקפד. בתעשייה שלנו, מספיק שהצלחת במוצר אחד".
- ועדיין, יש מחשבות על תשובה שלילית?
"ברור שתהיה אכזבה לכולם אם המוצר המשמעותי לא יצליח, אבל אני לא רואה מצב שבו אפוסנס לא תצליח במוצר כלשהו. לטווח ארוך, אני חושב שיש לנו סיכויי הצלחה טובים מאוד".
- יש חששות כלכליים?
"לשמחתי, בזכות כמה מהלכים עסקיים נכונים ותזמון נכון, מימון הוא לא החשש שלנו. יש לנו כסף לשלוש השנים הקרובות ובעלי מניות עם גב חזק".
גמידה סל

תורת התאים
הוקמה: 1998
מיקום: הר חוצבים, ירושלים
מייסדים: טוני פלד (היום המדענית הראשית בחברה) וד"ר אבי טרבס מהמרכז הרפואי שיבא
מנכ"ל: ד"ר יעל מרגולין
משקיעים בולטים: אלביט מדיקל טכנולוגיות, כלל תעשיות ביוטכנולוגיה, טבע, IHCV
גיוס הון: 42 מיליון דולרים (על-פי נתוני IVC)
מועד האירוע הקובע: תוצאות ניסוי שלב III כנראה ברבעון השלישי של 2012, ולכל היותר עד סוף השנה
ד"ר יעל מרגולין, מנכ"לית גמידה סל, חולמת על קו הסיום. "להביא תרופה לשוק זה הישג שלא רבים מגיעים אליו", היא אומרת. "כל מדען וכל בעל תפקיד בחברת פיתוח תרופות חולם על הרגע הזה. התהליך מהמעבדה לשוק הוא תהליך מאוד ארוך, מסובך ויקר, ולפעמים גם כואב. החלום להגיע לקו הגמר הוא ודאי חלק ממה שמוליך אותנו מיום ליום".
החברה שמובילה מרגולין פועלת לפיתוח טיפול תרופתי לסרטן הדם על בסיס תאי גזע, באמצעות טכנולוגיה המאפשרת להרבות את מספר תאי הגזע בדגימה של דם טבורי, תוך כדי שיפור הצפיפות שלהם. אם כיום מספיקה כמות תאי הגזע בדגימת דם טבורי לטיפול רק בחולים שמשקלם עד 45 קילוגרמים, כלומר בעיקר בילדים, הרי שלאחר הגדלת מספר התאים, השאיפה היא שניתן יהיה לטפל גם באדם מבוגר החולה בסרטן הדם.
גמידה סל כבר הקימה עם טבע מיזם משתף לשיווק המוצר לכשיגיע לשוק, וכעת נותר "רק" לצלוח את הניסויים הקליניים, ולקוות כי הם יספיקו לרישום מול ה-FDA. לוח הזמנים הוא כזה שאם הכול ילך לפי התכנון, החברה תוכל לרשום את המוצר לשיווק כבר ב-2013.
"אני לא מצפה לנקודת שיא שאחריה נוכל כולנו לנוח על זרי הדפנה", אומרת מרגולין. "גם אחרי שנסיים את הניסוי, יחל המירוץ לרישום המוצר, ואחר כך ייצורו ושיווקו. אולם לפעמים אנחנו אומרים, בואו נעשה לנו אתנחתא, נטפח לעצמנו על השכם, כי זה בכלל לא טריוויאלי שהגענו גם עד כאן".
הניסוי של גמידה סל מבוצע ללא קבוצת ביקורת אלא מול נתונים היסטוריים. לכן, בניגוד לרוב הניסויים, הנתונים אינם חסויים לחלוטין. עם זאת, מרגולין מדגישה: "אסור לנו לאסוף את הנתונים ולנתח אותם. אסור לנו לשוחח עם החולים או עם הרופאים, ואנחנו לא באמת יודעים מה תהיה התוצאה".
היא מקפידה לציין כי כבר נרשמו הישגים. "גם בתוך הניסוי הקליני, כבר הצלנו אנשים", כך מרגולין. "אסור לנו לדבר איתם, אבל אנחנו מקבלים פידבקים חד-כיווניים מהרופאים, וזו תחושה מדהימה. על אותו משקל, כשמת חולה בניסוי, זו הרגשה נוראית, אפילו שלא הכרנו אותם. גם אם הניסוי יסתיים בהצלחה מסחררת, עדיין מדובר במחלת הסרטן, וחלק מן הנבדקים מתים".
- ברמה היומיומית, המחשבה על הצלת חיים מדרבנת אותך להישאר עוד שעה ולא ללכת הביתה?
"ברמה היומיומית המנוע הוא ההנאה מהעשייה ומהעבודה עם האנשים שהם אינטליגנטיים, יצירתיים מאוד וחדורים באמונה במה שהם עושים. ברמה שמעל, נכון שכיוון שמדובר במוצר מציל חיים, זה נותן מוטיבציה".
- איך מתמודדים עם רגעים שבהם נראה שהגעתם למבוי סתום טכנולוגי או לבעיה לוגיסטית בלתי פתירה?
"הרגעים האלה נדירים כי הצוות מאוד יצירתי, גם בפתרון של בעיות טכניות וגם בהתמודדות עם אתגרים אחרים. אומרים שתמיד צריך להסתכל על קשיים בתור אתגרים, אז הפריבילגיה שלי היא שיש לי צוות שעוזר להתמודד בצורה כזו. אני לא לבד. אנחנו נסמכים מאוד זה על זה.
"בחברה עובדים 38 אנשים, ואני מנהלת אותם בצורה מאוד שקופה ומעורבת; זה לא השתנה כשגדל המספר, ואני מקווה שזה לא ישתנה גם בחברה של מאה אנשים. בניהול מעורב צריך להשקיע, זה לא קורה מעצמו: מעבר לשיחות המסדרון אני נפגשת מדי פעם על כוס קפה גם עם עובדים שלא מדווחים אליי ישירות. כמו כן אנחנו מציגים פעם ברבעון תוכניות עבודה, ומי שמציג הוא לאו דווקא המנהל אלא חבר בקבוצה, ואז כל אחד יודע מה החברים שלו עושים".
- איפה המשפחה שלך בכל התהליך?
"הם מאוד מעורבים. אני משתפת גם בתמונה הכללית וגם בהישגים ובאתגרים ספציפיים. הילדים שלי אמנם גדולים, אבל מדי פעם קורה שעובדים מהחברה רוצים שנגיע לבית ספר כדי לספר על הפעילות ועל הטכנולוגיה שלנו. אנחנו משתפים פעולה בשמחה".
- חשבת מה יקרה אם התוצאות לא יהיו טובות?
"לא, אני לא חושבת על הדבר הזה. בנינו תרחיש למצב הפסימי, אבל אני לא עסוקה בתסריט הזה ביומיום. ברמה האסטרטגית, חשוב להגיד שגם אם המוצר ייכשל, יש לנו מוצרים אחרים".