כשאנחנו חושבים על זיקנה, מחלת האלצהיימר היא אחת האסוציאציות המפחידות, בשנים האחרונות האפשרות שעד שנגיע לגיל הרלוונטי כבר יפתחו תרופה הייתה ריאלית בערך כמו האפשרות שנכדינו לא יצטרכו ללכת לצבא. התרופות הספורות שקיימות היום בשוק, כולל אחת שפותחה בישראל, יכולות להאט את התקדמות המחלה בכמה חודשים, אך אין בהן פתרון אמיתי.
מיליארדים רבים של דולרים מובטחים עדיין לחברה הראשונה שתצליח לפתח תרופה משמעותית, שכן מדובר בשוק ענק, ובכל זאת, בשנתיים-שלוש האחרונות צמצמו חברות הפארמה הגדולות את מאמציהן בתחום זה. הן פשוט התייאשו לאחר שנחלו סדרה של כישלונות חרוצים בניסויים מתקדמים בתרופות שתלו בהן תקוות רבות. כל ניסוי כזה עלה מאות מיליוני דולרים.
אחרי הכישלונות, התפיסה הרווחת הייתה שכנראה איננו מבינים באמת את מנגנון המחלה. אבל לאחרונה, ממש בחודשים האחרונים, ניכרים ניצנים של תקווה שמעוררים מחדש את השוק הזה.
המפתח: התערבות מוקדמת
החברות שהציגו את התוצאות הנחשבות מעניינות ביותר הן אלי לילי וביוג'ן. הראשונה הייתה גם אחת הנכשלות הגדולות של 2012, אך חזרה במהירות למשחק.
למעשה, אלי לילי ספגה שני כישלונות: תרופה אחת שלה, Semagacestat, שניסוי בה הסתיים ב-2010, לא רק שלא הצליחה לעצור או אפילו להאט את המחלה, לפי הנתונים ייתכן שהיא אף החמירה אותה. התרופה השנייה, solanezumab, לא הצליחה להראות השפעה מובהקת בניסוי שנערך באלפים רבים של חולים. אולם חוקרים של החברה הרגישו שיש בנתונים יותר מכפי שנראה לעין תחילה, וב-2012 הם הסתגרו בבניין בקמפוס לילי שנקרא "המערה" והחלו לבחון את הנתונים לעומק, בתקווה שיימצא דפוס חיובי כלשהו. לבסוף השתכנעו שלתרופה יש השפעה אמיתית, אך רק על חולים שקיבלו אותה כשהיו בשלבים מוקדמים מאוד של המחלה.
ב-2013, החליטה לילי להמשיך בניסוי ייחודי: בין כל החולים שהשתתפו בניסוי המקורי נבחרו אלה שמחלתם הייתה בשלב מוקדם (יותר מאלף חולים). מחציתם כבר קיבלו את התרופה בניסוי המקורי ומחציתם קיבלו תרופת דמה. בניסוי החדש נתנו את התרופה לכולם, וכעבור שנתיים, בוצעה השוואה בין הקבוצות. המטרה הייתה לראות אם מי שהחל לקבל את התרופה מאוחר (כי בניסוי עצמו היה בקבוצת הפלצבו) נמצא במצב פחות טוב ממי שהחל לקבל אותה מוקדם יותר.
התוצאות שפורסמו לפני כמה שבועות נותנות סיבה לאופטימיות, אך עדיין אינן מצדיקות יציאה במחולות ברחובות. אכן נמצא הבדל מובהק בין הקבוצות, ואלו חדשות מצוינות. אולם העובדה שהניסוי אינו רנדומלי וכפול סמיות (כלומר, החולים ידעו באיזו קבוצה הם) מוריד מכוחו. החברה צפויה לפרסם תוצאות נוספות מניסוי חדש ב-2016.
חברה שהציעה תוצאות חדשות לגמרי אך ראשוניות יותר היא ביוג'ן. היא הראתה בניסוי בקרב 166 חולים שתרופה שלה משפרת את מצבם הקוגניטיבי של החולים. גם במקרה הזה התוצאות הן מעט "טריקיות": במינון בינוני ונמוך התרופה לא עזרה. החוקרים מצאו כי התוצאה טובה יותר ככל שהמינון גבוה יותר ושהמגמה הזאת היא מובהקת. גם בניסוי של ביוג'ן, חולים שטופלו בשלב מוקדם יותר של המחלה השיגו תוצאות טובות יותר. ביוג'ן נערכת להיכנס כעת ישירות לניסוי שלב III, בכ-1,350 חולים, והתוצאות יתקבלו רק בעוד כשנתיים-שלוש.
ניסוי כמו זה שמתכננת ביוג'ן נחשב קטן וקצר יחסית למה שדרשו הרשויות הרגולטוריות בעבר מניסויים בתרופות לאלצהיימר. יונה גפן, מנכ"ל חברת אברהם פארמה הישראלית, המפתחת גם היא תרופה לאלצהיימר (ראו מסגרת), מסבירה: "עד 2013, רשות המזון והתרופות האמריקאית (FDA) דרשה שניסויים בתרופות האמורות לפעול בשלבים הנחשבים מקדימים לאלצהיימר (MCI - הפרעות קוגניטיביות קלות), יוכיחו שניתן למנוע את הידרדרות המחלה עד כדי אבחון של אלצהיימר ממש. זהו ניסוי שדורש הרבה מאוד שנים והרבה מאוד חולים, כי ממילא לא כל החולים ב-MCI יידרדרו לאלצהיימר, ואלה שכן - זה יכול לקרות להם כעבור שנים רבות, ולכן קשה להראות הבדל בין הקבוצות.
"כמו כן, עד 2013 הניסויים היו חייבים לכלול נוסף על מדד קוגניטיבי (מבחן זיכרון וחשיבה) גם מדד קליני (חוות דעת של רופא ומטפל עיקרי שיש הידרדרות במצבו של החולה). אלו נתונים שקשה יותר לאסוף והם גם רגישים יותר להשפעת פלצבו. לאחר כישלונות מהדהדים של לילי ושל פייזר השתכנעה הרשות בטענת החוקרים שייתכן שההתערבות היום באלצהיימר היא מאוחרת מדי, והיא התירה לבצע ניסויים בחולי MCI ועם שאלון קוגניטיבי בלבד".
ההנחיות הללו מעודדות חברות רבות לשוב ולבחון תרופות פוטנציאליות לאלצהיימר בקרב חולים בשלבים מוקדמים . חברת מרק אמורה לפרסם ב-2018 תוצאות מניסוי שלב III גדול בחולי MCI; פייזר נמצאת בניסוי שלב II בכמה מאות חולים שאמור להסתיים עד סוף השנה; ג'ונסון אנד ג'ונסון חתמה לאחרונה על עסקה לפיתוח מוצר שהיא קוראת לו "חיסון נגד אלצהיימר" ונמצא בשלב מוקדם של הניסויים.
שתי אסכולות וקוקטייל אחד
אחד האתגרים הגדולים בפיתוח תרופה לאלצהיימר הוא הבנת מנגנון המחלה, והיום קשה לדעת אם אנחנו בכלל קרובים לפיצוח. המנגנון החשוד המיידי, שלפיו פותחו רוב התרופות עד היום, נקרא "מנגנון צברי הבטא עמילואיד". אנחנו יודעים היום שכאשר בוחנים מוח של חולה אלצהיימר שנפטר מגלים כמות חריגה של חלבוני בטא עמילואיד שנדבקו זה לזה ויצרו משקעים קשיחים (פלאקים). גם באנשים מבוגרים שאינם לוקים באלצהיימר יש פלאקים כאלה, אך בחולי אלצהיימר יש הרבה יותר מהם, בעיקר באזורים במוח הקשורים לזיכרון. התופעה תוארה כבר על ידי ד"ר אלויס אלצהיימר שאפיין את המחלה בתחילת המאה ה-20. נראה שצברי החלבונים, הפלאקים, חונקים את תאי המוח ומונעים את תפקודם התקין.
בטא עמילואיד הוא חלבון טבעי ורצוי במוח. הבעיה מתחילה כשהחלבונים מתחילים לחבור זה לזה ליצירת המשקעים החריגים. את התופעה הזאת ביקשו התרופות למנוע, בגישות מגוונות. מיליארדי דולרים הושקעו בתקיפת הפלאק הבטא-עמילואידי, ללא הצלחה, עד שעלתה השאלה אם הוא הגורם למחלה. אולי הוא מופיע במחלה אך אינו גורם לה? אולי הוא בכלל מנגנון הגנה של המוח מפניה ופגיעה בפלאקים רק תחמיר את המצב? ואולי הפלאק כן גורם למות התאים, אבל אם מנסים לפרק אותו כשהוא כבר נמצא, זה מאוחר מדי וצריך למנוע את היווצרותו?
שתי התרופות של אלי לילי ושל ביוג'ן פועלות בגישה האחרונה, כלומר תוקפות את הבטא עמילואיד כמו התרופות שנכשלו, אבל בחולים בשלבים הרבה יותר מוקדמים, ואולי באפקטיביות רבה יותר. ביוג'ן הראתה שחולים בקבוצת הטיפול שלה מציגים הרבה פחות פלאקים מאשר בקבוצת הביקורת.
"בגישת העמילואיד בטא הושקע כל כך הרבה מאמץ, שהחוקרים פשוט לא מוכנים לנטוש אותה ומקווים מאוד שמשהו יקרה", אומרת פרופ' אילנה גוזס מאוניברסיטת תל אביב, שפיתחה בעבר תרופה מהאסכולה המתחרה, התולה את האשמה בחלבון בשם TAU (טאו). "היום אני כבר לא כל כך בטוחה שהסוד הוא לא בעמלואיד בטא ולא בטאו".
גם חלבון טאו חובר לחלבוני טאו אחרים ליצירת מבנים חריגים בחולי אלצהיימר. החשד הוא שהמבנים הללו לא רק מפריעים לתפקוד התקין, אלא שהטאו שיוצר אותם נלקח ממקומות שבהם הוא דרוש, למשל מצינוריות קטנות בתאי העצב. בהיעדר טאו תקין הצינוריות קורסות ולא מאפשרות תקשורת בתוך התא. חוקרים רבים סבורים שכדי לתקוף את האלצהיימר יש לשלב בין תרופה נגד עמילואיד בטא ובין תרופה נגד טאו. כך חושב, למשל, פרופ' מוסא יודעים מהטכניון, שפיתח את התרופה אזילקט לפרקינסון (מחלה הדומה במובנים רבים לאלצהיימר). היום נמצאות בפיתוח שתי תרופות שלו לאלצהיימר: הוא שותף בפיתוח של אברהם פארמה שהזכרנו ובפיתוח תרופה אחרת בשם M-30 בחברת אביטל פארמה שבשליטתו. "כנראה התרופות נגד בטא עמילואיד לא פעלו היטב משום שתקפו רק אותו. יש לתקוף אותו ואת הטאו במשולב וכן לשלב מנגנונים נוספים, בדיוק כמו שעשו בתחום האיידס ועושים היום גם בתחום הסרטן - קוקטיילים של תרופות הם הפתרון ולא תקיפה של מנגנון אחד".
הכוח של אמנות: טיפול זה לא רק תרופות
בהעדר תרופה, עמותת עמדא, העמותה לאלצהיימר ומחלות דומות בישראל, שמה לה למטרה לדאוג לאיכות החיים של החולים באלצהיימר ובני משפחותיהם, להעלות את המודעות למחלה ולתמוך במחקר. "אחת משיטות הטיפול המשמעותיות שלנו היא לשוב ולחבר את החולה לתרבות על מגוון פניה", אומר מנכ"ל העמותה, גרי רוט. "צריכת תרבות מזכירה להם חוויות מצעירותם".
אחד מפיתוחי העמותה הוא תוכנת "בכורסה עם פיקאסו". מדובר באוסף תמונות, ולצד כל אחת מהן מופיע סיפור על היצירה ושאלות הכוונה למטפל - כיצד ליצור שיחה עם האדם הדמנטי כך שהיא תזכיר לו משהו מחייו - ביתו, עיר מגוריו, קבלת שבת בביתו וכדומה. "אלה דברים השמורים עד שלבים יחסית מאוחרים של המחלה", אומר רוט.
כשאפשר, לוקחים את המטופלים לביקור במוזיאון. "הבאנו קבוצה משכונת התקווה לתערוכה על ת"א של פעם והראינו תמונות ממלחמת הקוממיות, והנה קמה אישה שחצי שנה כבר לא שמענו את קולה ואמרה בקול צלול שהשתתפה באירוע הזה. המשפחה שלה הייתה כל כך שמחה", מספר רוט.
גם זיכרון מוזיקלי נשמר עד שלבים מאוחרים של המחלה. "כשחילקנו לקשישים אייפודים, ראינו שאנשים שהיו מרותקים לכיסא ומנותקים ממש קמו לתחייה כשהשמיעו להם מוזיקה שמזכירה להם את הבית. זה עוזר בטיפול באנשים שיש בעיה לקלח אותם, שיש קושי להאכיל אותם. המוזיקה מסיחה את דעתם", אומר רוט. "אחת המטופלות שלנו הייתה במצב מאוד ירוד, בקושי דיברה. השמענו לה מוזיקה שהזכירה לה את ילדותה, והיא התחילה לדבר בשצף קצף, ורק על סקס. היינו מאושרים שהיא מדברת".
פריחה ישראלית בחקר האלצהיימר
הניסוי של אברהם פארמה
לאחרונה פרסמה החברה, המתבססת על מחקריהם של פרופ' מרתה ויינשטוק רוזין (ממציאת האקסלון) ופרופ' מוסא יודעים, תוצאות ביניים מעניינות מאוד מניסוי ב-210 חולים שסבלו מ-MCI. התרופה של החברה מראה מגמה חיובית במצב הקוגניטיבי של המטופלים, והיה הבדל מובהק באובדן נפח המוח של המטופלים (ירידה בנפח המוח היא סימן למחלה דמנטית). כעת מחכים לפרסום התוצאות הסופיות בעוד כשנה. המוצר משלב בין האקסלון המוכר לבין רכיבים מהתרופה של טבע לפרקינסון, אזילקט. לדברי מוסא יודעים ויונה גפן, השילוב הזה יוצר גם אפקט אנטי-דלקתי המגן על תאי העצב מפני מוות, ללא תלות בגורם המאתגר אותם ומסכן אותם. כמו כן, אומר יודעים, בשילוב הזה יש רכיב שהופך את חלבון העמילואיד המסוכן ל"עמילואיד טוב", בעל השפעה חיובית.
החומר של פרופ' יודעים
מוסא יודעים מפתח גם חומר בשם M-30 המשלב את האקסלון, האזילקט ועוד רכיב הקשור לצבירת ברזל. "ידוע שבמחלות ניווניות של המוח לעתים קרובות נצבר ברזל באתר במוח שקשור להיווצרות המחלה. התרופה שלנו כוללת גם רכיב שמונע את הצטברות הברזל", הוא אומר. המוצר עדיין לא נמצא בניסויים קליניים.
הגלגולים של מחקר פרופ' אילנה גוזס
המחקר של גוזס עמד בבסיס המוצר שפיתחה חברת אלון ת'רפויטיקס והשיג תוצאות מעניינות ב-MCI, אך במקום לאלצהיימר הוא נרשם לטיפול במחלת יתום בשם PSP, בהנחה שמסלול זה יהיה קל יותר. אך המוצר נכשל ולא פותח מאז. גוזס העבירה בינתיים חלק מהידע שלה לחברת קורוניס פרטנרס, המפתחת את המוצר דווקא לסכיזופרניה. "אנחנו מנסים לשמור על הדינמיות והשלמות של הצינוריות הנמצאות בתא העצב ומחזיקות את השלוחות הארוכות מאוד של תאי העצב. החומר שאנחנו עובדים עליו מגייס את החלבון טאו וחלבונים אחרים לשמירה על הצינוריות לפני שנגרם הנזק", אומרת גוזס. התרופה עדיין לא עברה את שלב הניסויים בבני אדם וכעת היא מחפשת השקעות.
הנוגדן של פרופ' בקה סלומון
פרופ' סלומון פיתחה נוגדן נגד בטא עמילואיד והוא עמד בבסיס ניסוי ענק של חברת פייזר, שלמרבה הצער נכשל. אבל סלומון ממשיכה לפתח מוצרים דומים המשלבים נוגדנים נגד בטא עמילואיד ונגד חלבון טאו וכן מוצרים נוספים.
הפעילות של Xonovo
חברת Xonovo שהקים רפי גדרון והיום היא חלק מהחממה הטכנולוגית FutureX מפתחת תרופה נגד החלבון CRMP2, שעד היום לא היה מטרה בתרופות שנוסו ונכשלו. ניסויים בבעלי חיים (הנחשבים באלצהיימר מודל לא מוצלח במיוחד) הראו שהחומר מאט הידרדרות קוגניטיבית.
טיפול בגירוי מוחי
בישראל פועלות שתי חברות העוסקות בגירוי מוחי לטיפול באלצהיימר - ברייסוויי ונוירוניקס. הרעיון מאחורי הטיפול הוא שגירוי מוחי יכול לחזק את התאים במוח ואת הקשרים ביניהם באופן שהופך אותם עמידים יותר בפני מנגנון המחלה.
שיקום בעזרת תאי גזע
החלום הגדול הוא לשקם תאי מוח שכבר נפגעו, ואולי ניתן יהיה לעשות זאת בעתיד באמצעות תאי גזע. במחקר בראשות פרופ' דני אופן וד"ר עדי שרוסטר מאוניברסיטת תל אביב, הצליחו החוקרים לייצר בעכברי מעבדה תאי מוח חדשים באזורים שנפגעו מאלצהיימר. כמה חוקרים ישראלים נוספים פועלים בתחום.
התקוות הראשוניות של טבע
לחברת טבע אין היום מוצר מתקדם לאלצהיימר, אולם יש לה תוכנית תמיכה במחקר ישראלי בתחום המוח בשם NNE, הרשת הלאומית למצוינות בחקר המוח, שבמסגרתה מתקיימים גם פרויקטים בתחום הזה. אחד מהם הוא של דנה בראון, חוקרת במעבדה של פרופ' אורי אשרי הפועלת ליצירת מפות מוח המתחקות אחר הפיזור של כל החלבונים הרלוונטיים למחלה בקרב חולים ובריאים. באמצעות השוואת המפות אפשר להשיג גם אבחון מוקדם וגם להתחקות אחר התקדמות המחלה כדי להבין את המגנון שלה. "בינתיים גילינו שאפילו כמה חודשים לפני שצברי החלבונים מתחילים להתפתח חלבונים חיוניים עוברים ספיחה לתוך הצברים ואז התא שממנו נשאבו החלבונים החיוניים מתחיל לגלות סימני מצוקה. אולי זה מנגנון המחלה", היא אומרת. "המטרה היא שבהמשך נוכל לנבא לפי המפות אילו חלבונים צריכים להופיע בגוף כאשר המחלה מתחילה, ועל ידי דגימה מהאף, העור או המעיים, אולי ניתן יהיה לאבחן את המחלה לפני שהיא גורמת נזק. באמצעות טבע נוצר שיתוף פעולה עם חוקר המפתח מולקולות שאמורות למנוע את היווצרות הצברים, ונבחן יחד מהי בדיוק ההשפעה של המולקולה שלו על התאים".
חוקר אחר בתוכנית הוא שחר ברבש, ממרכז אדמונד ולילי ספרא למדעי המוח באוניברסיטה העברית. ברבש חוקר כיצד ניתן להשפיע על אלצהיימר באמצעות מיקרו-RNA - המולקולות השולטות על התבטאות של גנים. עד היום התרופות שנוסו ונכשלו כוונו לחלבונים. "איננו יודעים עדיין מהם הגנים הגורמים לאלצהיימר, אך המדע מכיר גנים שעוזרים לשמור על תאי עצב מפני מוות ופעילותם מתאפשרת על ידי מיקרו-RNA מסוימות, שרמתן יורדת בחולי אלצהיימר. הקשר עם טבע והעובדה שאני פועל במעבדה של פרופ' חרמונה סורק שכבר פיתחה בעבר תרופות אפשרה לי לחשוב על המחקר שלי כתרופה פוטנציאלית".
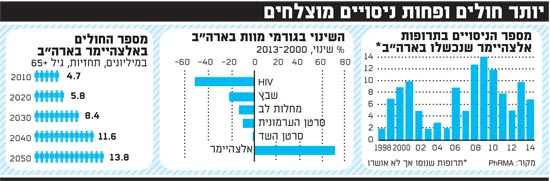
יותר חולים ופחות ניסויים