הדרישה הראשונה שמבקש האדם הסביר מעולם הרפואה היא להאריך חיים. הבקשה השנייה היא כנראה למות צלול. אולם, ההצלחות הרפואיות בטיפול בגוף האדם בשנים האחרונות לא לוו בהצלחות שוות ערך בתחום חיי המוח. כך יוצא שאנחנו יותר ויותר מאריכים חיים, אך מי שיחצה את גיל 85 יעלה את סיכוייו ללקות במחלת האלצהיימר ל-15%. ומי שיעבור את גיל 90 - ל-20%. הסיכון לדמנציה מכל הסוגים אחרי גיל 90, כולל אלצהיימר, מגיע לכ-30%, כשנתונים אלה לא כוללים את הירידה ההדרגתית הצפויה באיכות הזיכרון ובתפקוד בגיל המבוגר, שאינה מתקראת "דמנציה".
אלצהיימר מוגדרת כמחלה, וכנראה אינה חלק מן הבלאי הטבעי של הגוף. שינויים בסגנון החיים אמנם הובילו להארכת תקופת הצלילות ולדחיית הופעת מחלת האלצהיימר, אולם הניסיון של עולם התרופות להצטרף לחגיגה - נכשל. חברות התרופות נכשלות שוב ושוב בניסיון לעצור או אפילו להאט את המחלה, והיקף ההשקעות הכושלות בתחום מגיע לכ-100 מיליארד דולר. למעשה, מחלת האלצהיימר נחשבת ל"בית קברות לתרופות".
האם חברת התרופות ביוג'ן, שהודיעה השבוע כי מצאה תרופה אחרי מאבק ארוך ודרמטי אכן תזכה בכל הקופה? לא כל כך מהר, אומרים האנליסטים והמשקיעים המובילים בשוק.
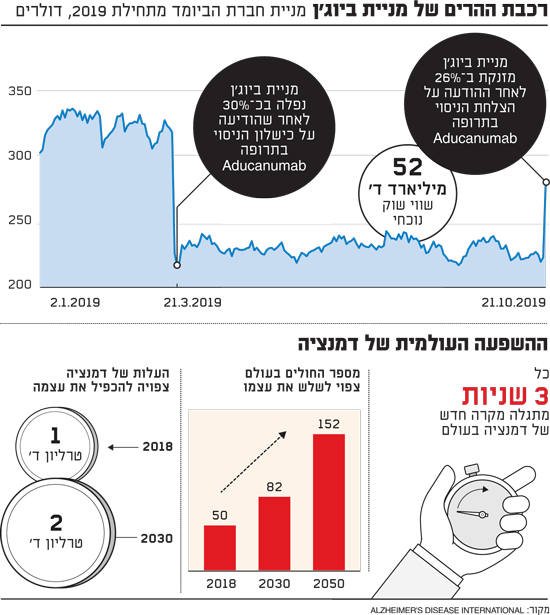
ההשפעה העולמית של דמנציה - אתר
הניסוי שהתהפך והאנליסטים החשדניים
ביוג'ן הדהימה את השוק כשהכריזה שניסוי בתרופה לאלצהיימר בשם aducanumab שהוכרז במרץ האחרון ככישלון מוחלט עד כדי ויתור על כל תוכניות הפיתוח למוצר זה - הוא בעצם הצלחה. מניית החברה נסקה באותו יום ב-26% והביאה את החברה לשווי של 52 מיליארד דולר.
איך הופך ניסוי כושל להצלחה? באמצעות ניתוח מעמיק יותר של התוצאות. האם זה מספיק כדי להפוך מוצר שפיתוחו הופסק לתרופה קיימת בשוק? ביוג'ן משוכנעת שכן.
החברה הודיעה שהחליטה, תוך התייעצות עם ה-FDA, רשות המזון והתרופות של ארה"ב, להגיש את המוצר לאישור שיווק על בסיס תוצאות הניסוי הקיימות בתחילת 2020.
עם זאת, המשקיעים והאנליסטים כאמור עדיין קצת סקפטיים. הם טוענים כי ההחלטה של ה-FDA להסכים לקבל את המוצר לבדיקה עדיין אין בה הבטחה לאישור. על דבר אחד כולם מסכימים - המוצר שאמור היה כבר לראות את סופו, שב לתחייה וקיבל סיכוי נוסף.
אגב, יש כיום רק ארבע תרופות קיימות בעולם לטיפול במחלת האלצהיימר (כולל אחת שפותחה על ידי החוקרת הישראלית פרופ' מרתה ויינשטוק רוזין), אך אף אחת מהן לא אושרה בעשור האחרון. השוק משווע למשהו חדש. כל התרופות שנמצאות בשוק מאטות במקצת את התקדמות המחלה, אך בוודאי שלא עוצרות או מרפאות אותה. אם תימצא תרופה יעילה יותר, היא תזכה לחיות בשוק ענק של עשרות מיליוני חולים שרק משוועים למעט תקווה.
התרופה עדיין רחוקה מאישור
איך התהפכו התוצאות של ביוג'ן? החברה בעצם ערכה שני ניסויים רחבי היקף (ניסויי שלב III, שהוא השלב האחרון של ניסויים שמבוצע לקראת שיווק) ב-aducanumab. ה-FDA לפעמים דורש לערוך שני ניסויים זהים כדי לוודא שהתוצאות אמינות ואינן תוצאה של מזל מקרי. החברה בחרה לערוך את שניהם במקביל במטרה לחסוך זמן.
כל ניסוי קליני גדול שנערך מול ה-FDA צריך לעבור מעת לעת ביקורת של ועדה חיצונית מייעצת. תפקיד הוועדה הוא לראות את תוצאות הניסוי עד לאותה נקודה, ולהחליט האם הניסוי נראה מבטיח ואם יש טעם להמשיך. אם לא - חבל לטרטר את החולים. במקרה הזה הוועדה קבעה, על פי נתוני הביניים, שהסיכוי להצלחת הניסויים קלוש ושיש לעצור אותו.
ביוג'ן הודיעה על מות המוצר. אולם, כמו חברות תרופות אחרות, היא ביצעה ניתוח בדיעבד של התוצאות לשם הפקת לקחים. זהו חלק מהאחריות החברתית של חברת תרופות לעולם המדעי. הניתוח כלל נתונים מחולים רבים יותר מכפי שראתה הוועדה המייעצת. בניתוח החדש נמצא כי אחד הניסויים עמד ביעד העיקרי. ניסוי שני אמנם נכשל, אבל בתת-קבוצה של חולים עם אלצהיימר קל יותר, שקיבלו מינון גבוה יותר, נרשמה הצלחה.
החברה דיווחה כי לאחר התייעצות עם ה-FDA הוחלט להגיש את המוצר לאישור. בשלב זה, לא ברורה מה היא משמעות ההסכמה של ה-FDA לקבל את התוצאות. מצד אחד בטוח שהרשות חושבת שיש משהו אמיתי בנתונים, אך מצד שני זו ממש לא הבטחה לאשר את המוצר. ה-FDA עדיין יכולה לדרוש מן החברה ניסוי נוסף, או לאשר את המוצר לקבוצה מוגבלת של חולים או אפילו לדחות את התרופה לגמרי. כרגע רב הנסתר על הגלוי לגבי תוצאות הניסוי, ומידע נוסף יתברר כשה-FDA ישמיע את דברו, במהלך 2020.
ב-2018 כבר הודיעה ביוג'ן כי היא תגדיל את הניסויים ותשנה את הפרוטוקול, על רקע "גיוון" בתגובות החולים לתרופה. הגדלת ניסוי תוך כדי התרחשותו היא בדרך כלל סימן שתוצאות הביניים אינן מובהקות מספיק. ובמרץ השנה אכן נראה היה כי הסימן הזה אכן הקדים את המכה.
השבוע כאמור, סיפקה ביוג'ן פרשנות הפוכה. לדבריה, החולים שראתה הוועדה המייעצת, שהפסיקה את הניסוי, הם אלה שנרשמו לניסוי מוקדם - ולכן לא נהנו משינוי הפרוטוקול. זאת הסיבה שהוועדה המייעצת הגיעה למסקנתה המוטעית - כך אמרה החברה במפורש בשיחת הוועידה שלה עם המשקיעים.
עם זאת, גם אם המוצר יאושר, עדיין לא ברור אם מידת התועלת שלו בעיני הרופאים תהיה כזו שמצדיקה את השימוש בו בכל חולי האלצהיימר, או רק בתת-קבוצה קטנה. אנליסטים מציינים כי העלייה בשווי של ביוג'ן בעקבות ההצלחה מביאה בחשבון שהתרופה תהיה רבת-מכר. גורם נוסף שיש לשקול הוא חברות הביטוח - איזו רמת שיפור בחולים תידרש כדי לשכנע אותן לשלם עבור התרופה?
המלחמה בחלבונים שמצטברים במוח
ביוג'ן עשתה לשוק היכרות עם המוצר aducanumab ב-2015, לאחר ניסוי ראשוני מוצלח בכמה עשרות חולים. המוצר היה אחת התקוות הגדולות של החברה, בעיקר אחרי שמוצרים אחרים שלה לאלצהיימר נכשלו בזה אחר זה.
חלק מן המשקיעים, האנליסטים והרופאים בשוק הזהירו מראש כי המוצר משתמש במנגנון שכבר נוסה בעבר אין ספור פעמים ולא הצליח. המוצר תוקף חלבון שמצטבר במוחם של חולי אלצהיימר, בשם עמילואיד-בטא. מכיוון שלחולי אלצהיימר ישנה הצטברות של החלבון בעוד שלאנשים בריאים אין, נראה כי הוא חלק מן המחלה.
מנגנון זה הותקף בעבר על ידי תרופות רבות אחרות, ללא הצלחה. אמנם אפשר שהתערבות מסויימת במנגנון הביולוגי תצליח, למרות שאחרות נכשלו, אולם בשנים האחרונות הופכים המדענים בתחום ליותר ויותר סקפטיים לגבי עצם התזה שהמנגנון הזה גורם למחלה. לפי טענה אחרת, מצבורי העמילואיד-בטא כבר נבנו, ופירוק שלהם לא ישיב לאחור את הנזק שכבר נעשה. רק מניעת הצטברות העמילואיד במוח מלכתחילה היא התרופה.
ביוג'ן היא דווקא מאמינה גדולה בהתערבות במנגנון העמילואיד-בטא, ובנתה את מוצרי האלצהיימר שלה סביב מוצר זה. בכירי ביוג'ן הצהירו בעבר כי הם מאמינים שהתערבות מוקדמת תוביל לתוצאות שהתערבות בשלבים מאוחרים של המחלה אינה יכולה להשיג. לכן החלה החברה בניסוי במוצר ה-aducanumab בחולים עם הפרעה קוגניטיבית קלה, שנמצאים בסיכון לפתח אלצהיימר. אולם, הניסוי הזה הופסק לאחר שהניסוי באותו המוצר באלצהיימר הוצהר ככישלון. כעת, ייתכן כי גם ניסוי זה יתחדש.
"אני מאמין שנמצא תרופה"
בראיון בלעדי ל"גלובס" ב-2018, אמר מנכ"ל ביוג'ן, מישל וונטסוס: "כיום, כאשר מאבחנים אלצהיימר, המשמעות היא שההידרדרות תחל בקרוב ותוביל בהכרח למוות. אנחנו מאמינים שהמחלה מתחילה לפעול עד 20-25 שנה לפני התסמינים הראשונים". הוא תיאר מודל טיפול שמתחיל לפעול לפני הופעת סימנים קליניים למחלה, כמו במקרה של טיפול ב-HIV ויתר לחץ דם.
עוד אמר אז וונטסוס, כי החברה מחוייבת להשקיע "הון עתק" לטיפול באלצהיימר, וכי תוכנית הפיתוח הזו היא מה שמדרבן אותו לקום בבוקר. "אני מאמין שנמצא את התרופה למחלה הזאת. אנחנו מהמרים עליה בגדול".
בתשובה לשאלה מה יאמר למשקיע שחושש מן הסיכון, ענה: "כשיש סיכון גבוה, דרושים מנהיגים וארגונים שיודעים לנהל את הסיכון. זה היתרון של ביוג'ן".
לרגע אחד, ישראל הייתה מעצמת אלצהיימר. אולי היא עוד תהיה
התרופה אקסלון לטיפול באלצהיימר, שאושרה לשיווק על ידי ה-FDA ב-2000, הייתה אחד החידושים האחרונים שהגיעו לשוק בתחום זה. מאז הוא דומם. המוצר שווק על ידי חברת התרופות נוברטיס, שרכשה אותו מן האוניברסיטה העברית, שם הוא פותח על ידי הישראלית פרופ' מרתה ויינשטוק רוזין.
על רקע ההצלחה הזו, והמובילות המדעית של האקדמיה הישראלית בתחום מחלות המוח, הפכה ישראל בתחילת העשור למיני-מעצמה בתחום האלצהיימר. מספר חוקרים ישראליים הצליחו להביא תרופות לטיפול באלצהיימר לשלבים מתקדמים של ניסויים קליניים, אחרי שניכרו בהם סימני יעילות בנסויים ראשוניים יותר. אולם, כמו בכל התחום, המוצרים נכשלו בזה אחר זה.
מוצר על בסיס מנגנון עמילואיד-בטא (המנגנון שעליו מושתת גם המוצר של ביוג'ן), שפיתחה פרופ' בקה סלומון מאוניברסיטת תל אביב, נרכש על ידי סינדיקט של החברות פייזר וג'ונסון אנד ג'ונסון. הוא נכשל ב-2012 בניסוי שלב III.
חברת אלון פארמה, שנסחרה בבורסה של טורונטו, פיתחה מוצר לטיפול בהפרעות קוגניטיביות שונות וביניהן אלצהיימר. החברה נכשלה ב-2013 בניסוי הראשון שלה במחלת מוח נדירה ולא המשיכה הלאה.
ויינשטוק-רוזין, שפיתחה את האקסלון, המשיכה להקמה של חברה נוספת בתחום, אברהם פארמה, יחד עם פרופ' מוסא יודעים, שפיתח את התרופה אזילקט לפרקינסון. החברה נכשלה ב-2012 בניסוי באלצהיימר, וב-2016 בהפרעה קוגניטיבית.
כל המוצרים הללו אמנם לא הצליחו, אולם הפיתוח הניח תשתית של ידע שעשויה לאפשר לישראל להצטרף למהפכה בתחום ברגע שתהיה פריצת דרך בתחום בעולם והכסף ישוב לזרום אליו.
חברת נוירונטיקס, המפתחת מכשיר לגירוי מוחי ואימון באמצעות משחק מחשב, אשר יחד אמורים לשפר את מצבם של חולי אלצהיימר, נשלחה הביתה על ידי ה-FDA השנה, בטענה כי הניסוי שהגישה לרשות לא הראה יעילות מספקת למוצר. החברה עורכת ניסויים נוספים.
מחברת התרופות מדיסון, המשווקת את מוצריה של ביוג'ן בישראל, לא נמסרה תגובה, אולם סביר כי מדיסון תשווק גם את התרופה הזו אם אכן תאושר ותגיע לישראל.
לתשומת לבכם: מערכת גלובס חותרת לשיח מגוון, ענייני ומכבד בהתאם ל
קוד האתי
המופיע
בדו"ח האמון
לפיו אנו פועלים. ביטויי אלימות, גזענות, הסתה או כל שיח בלתי הולם אחר מסוננים בצורה
אוטומטית ולא יפורסמו באתר.