אם היינו צריכים להרכיב את המוח, ודאי היינו הולכים לאיבוד בניסיון לחווט מיליוני עד מיליארדי תאים מסוגים שונים כך שיתקשרו זה עם זה באופן קוהרנטי ותקין. הדבר המדהים במוח הוא לא רק שהחיווט הנכון הזה אפשרי ויוצר בני אדם שהם תבוניים לעתים, אלא שהמוח עצמו אחראי לחיווט הזה בעצמו.
פרופ' ג'ושוע סיינס, מבכירי הנוירולוגים של אוניברסיטת הרווארד ועד לאחרונה ראש המרכז לחקר המוח באוניברסיטה, רצה לחקור איך המוח עושה את זה, מסיבות פרקטיות. מגיל צעיר הוא האמין שזה המפתח להבנת בריאות הנפש.
העניין שלו במחלות נפש הביא אותו כבר בתיכון למצוא משרה במעבדה למיקרוביולוגיה בבית החולים לילדים באפלו שבניו יורק, שחקרה את הקשר בין מחלות נפש לזיהומים חיידקיים.
"האינטואיציה שלי בתחילת הקריירה שלי, שהיא היום התפיסה מקובלת בתחום (אם כי זה עדיין לא הוכח), אמרה שבעוד שמחלות נוירולוגיות כמו אלצהיימר, פרקינסון או ALS נובעות מנזק לתאים, במחלות פסיכיאטריות כמו אוטיזם, דיכאון וסכיזופרניה הבעיה, לפחות בתחילת הדרך, אינה בתאים עצמם אלא בקשר ביניהם. באופן שבו הם עובדים יחד", הוא אומר בראיון לגלובס.
הלב של הלמידה והזיכרון
כדי לנסות להבין היכן הבעיה, סיינס ניסה קודם כול להבין איך נראה קשר נכון בין נוירונים איך הם בכלל מוצאים זה את זה ומתחברים ביניהם כדי ליצור את הרשת המסובכת שהיא המוח. מדוע נוירון מסוים מתחבר לנוירון אחד ולא לשני, ואיך הם בונים את הסינפסה, שבה מתרחשת התקשורת ביניהם.
סינפסה היא מעין חלל שמחבר בין סופו של תא עצב אחד לתחילתו של תא עצב אחר. כדי שתיווצר תקשורת בין תאי העצב, נוירון א' מפריש מהקצה הפולט שלו חומר כימי מסוים לתוך הסינפסה, ונוירון ב' אוסף אותו לקצה הקולט שלו. סוג החומר, כמותו, והמרחק בין הנוירונים משפיעים כולם על המסר שיעבור בין התאים.
מדוע בעצם המוח בנוי בצורה הזו של תאים וסינפסות?
"שאלה טובה, הרי אפשר היה שתאי העצב יהיה מחוברים זה לזה ישירות, ויעבירו חשמל ישירות ביניהם. פעם באמת חשבו שכך זה עובד. אבל היתרונות של סינפסות הם רבים. יתרון אחד הוא שיש להן כיוון. לכל תא יש צד קולט וצד פולט והמידע רץ רק בכיוון הזה, ולכן גם המידע בסינפסה עובר בכיוון אחד. כמו שלא נבנה מערכת הולכת מים שבה המים יכולים לזרום לשני הכיוונים, כך גם כדי שמידע יגיע ממקום למקום, יש יתרון שתהיה לו כיווניות.
"דבר נוסף, סינפסה יכולה לשמש כמעין מגבר. אם המוח היה מבוסס על מעגלים חשמליים בלבד, הסיגנל היה דועך לאורך הדרך. הסינפסה מהווה מגבר, כך שבנוירון הבא, שוב יש אות חשמלי מאוד חזק.
"אבל הדבר הכי חשוב הוא שסינפסות יכולות להשתנות בתגובה להשפעות חיצוניות. אם משתמשים בסינפסה הרבה, הסיגנל שהיא מעבירה יגבר. זהו הלב של יכולת הלמידה והזיכרון שלנו, אם כי אף אחד לא יודע בדיוק איך זה עובד. ראינו שינויים בסינפסות בחיות מעבדה כמו תולעים, זחלים וזבובים, אבל קשה לדעת בוודאות אם אותם חוקים חלים במערכת כל כך מורכבת כמו המוח האנושי, וגם הרבה יותר קשה לחקור את זה".
איך תאים מחליטים להתחבר
סיינס הקדיש את הקריירה שלו לשאלה איך הסינפסה נוצרת כך שהיא תהיה גם יציבה וגם גמישה. על תרומתו למחקר הזה, העניקה לו לאחרונה האוניברסיטה העברית בירושלים תואר ד"ר לשם כבוד לשנת 2022.
"התחלנו לחקור את הנושא במקום שקל יחסית להגיע אליו - במפגש בין תאי העצב לבין השריר, ולא במוח, כי אותו מאוד קשה לחקור", מספר סיינס. "ניסינו להבין איך נוצרת הסינפסה שמאפשרת לתא העצב לשלוח מסרים לשריר, וגילינו שכאשר הנוירון צומח לכיוון תא השריר, הוא מפריש חומר מסוים ואז השריר מבין שהוא צריך ליצור את החלק שלו בסינפסה ומפריש חומרים מסוימים חזרה. כך שני הצדדים יודעים שהסינפסה קמה.
"אמנם המידע שתאי העצב רוצים להעביר זורם בכיוון אחד - רק מתא העצב לשריר, אבל במקביל מתקיימת 'מטה-שיחה', שבה תא העצב והשריר מפרישים חומרים זה כלפי זה, כדי לחזק או להחליש את הסינפסה. בתחילת הדרך, כשהסינפסה נוצרת, השיחה מאוד ערה. עוד חומרים ועוד שינויים ועוד חומרים, עד שהסינפסה המתאימה נבנית. בבגרות, הקשר יציב יותר, אבל עדיין יכול להשתנות עד גבול מסוים".
אבל לסיינס הייתה משימה עוד יותר מורכבת - להבין איך תא יודע איזה תא נגדי עליו לפגוש. במוח ישנם מיליוני תאים, וכדי ליצור רשת שמעבירה מידע באופן משמעותי יש ליצור קשר אך ורק בין תאים מסוימים. "בשלב הזה עזבנו את חקר השריר ועברנו לחקר הרשתית של העין, שהיא מצד אחד נגישה ומצד שני היא מורכבת ממש כמו המוח כולו".
בעבר נאמר שהרשתית היא כמו מצלמה, אך התברר שהיא הרבה יותר מכך. "אפשר לומר שהיא כמו מצלמה עם תוכנת פוטושופ מאוד מורכבת", אומר סיינס. "והיא מכילה יותר ממאה נוירונים מסוגים שונים.
"אנחנו רואים שהתאים לפעמים נפגשים ונפרדים, אבל לפעמים הם נפגשים ומתחברים. חשבנו שאולי יש לכל תא את אוסף הכימיקלים שלו שהוא מפריש במפגש עם תא אחר, ואם יש התאמה - הם מחליטים להתחבר. וגילינו, לפחות בעכברים, שזה נכון: כאשר ערכנו את הגנטיקה של העכבר כך שנוירון מסוים לא יוכל להפריש חומר מסוים, לא נוצרו הסינפסות הצפויות. כאשר הזזנו גן מנוירון אחד לנוירון אחר, הסינפסות נוצרו במקום הלא נכון. כך זיהינו את אחד החומרים שהפרשתם יוצרת סינפסות רק בין שני תאים מסוימים. אני לא הממציא של התיאוריה הזאת, אבל עשיתי חלק מהעבודה שהוכיחה את זה".
רשתית העין כמודל למוח
לדברי סיינס, הוא וחוקרים נוספים מיפו את סוגי הנוירונים ברשתית ואת הגנים שלהם. "היום אנחנו יודעים אילו גנים יש בכל סוג של תא, וכשיודעים את זה, אפשר לצבוע אותם בצבעים שונים במעבדה ולראות איך הם קשורים זה לזה ואיך הם מתחברים. אז יש לנו את הגנטיקה של התא, מה הוא עושה ולמי הוא מתחבר. זו התחלה של פענוח המכונה הזו שנקראת הרשתית".
כבר היום יש לגישה הזאת פן יישומי. "אנחנו בוחנים התפתחות מצד אחד, ומחלות מצד אחר. אנחנו יכולים למפות רשתית של בני אדם אחרי המוות, למשל בני אדם שהייתה להם גלאוקומה. אנחנו יכולים לראות איזה תא מת בגלאוקומה, ומה היו השינויים הגנטיים שהוא עבר בדרך למוות הזה.
"בעבודה אחרת שעשינו בעכברים, פגענו בעצב הראייה שלהם ואז עקבנו אחרי התהליך שבו תאים מתים - שוב, בחנו איזה סוג תא מת ומה השינויים הגנטיים שהוא עבר בדרך למוות, ולא פחות חשוב מכך: איזה תא שרד זמן רב יותר מאחרים ומה הגנטיקה שלו. ברגע שיודעים זאת, אפשר להעביר את הגנים שנראים כמשפיעים לטובה על הישרדות גם לתאי העצב האחרים. ואנחנו באמת רואים שכשאנחנו עושים את זה בעכברים, אנחנו מצליחים להאריך את משך החיים של תאים שונים ברשתית גם במקרה של פציעה".
מחקר כזה יכול להוביל לטיפול בגלאוקומה?
"כן, וזה רק השלב הראשון. הרי תאי העצב של העין הם ממש כמו אלה של המוח. אם נבין אילו גנים משפרים שרידות של תאי עצב בתנאי קיצון או משקמים תאים כאלה אחרי נזק, אולי נוכל לעזור למגוון מחלות ניווניות של המוח (אלצהיימר, פרקינסון, ALS ועוד). יש לנו קולגה שהתחיל לבדוק כיצד השינויים האלה יכולים לעזור להגן מפני הנזק של פציעות בחוט השדרה, אולי אפילו לתקן אותן".
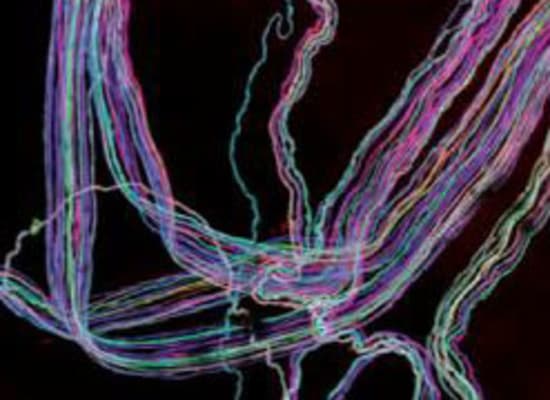
נוירונים של עכבר צבועים בטכנולוגיית Brainbow שפיתח סיינס / הדמיה: מתוך מחקר של סיינס
סיינס מסווג את התאים בין היתר באמצעות טכנולוגיה שפיתח, שנקראת Brainbow, המאפשרת לצבוע תאים בצבעים שונים, עד כדי תתי-גוונים מדויקים, כדי להבין את מבנה הרקמה. "לצערי אנחנו עדיין לא יכולים לסמן את התאים בצבעים לפי סוג, אבל אם אנחנו מסמנים תא אחד, אנחנו יכולים לראות לאן הוא הגיע במרחב, כמו שמסמנים חוט חשמל בצבע מסוים כדי לזהות אותו בתוך סבך של חוטים".
מה אתה חושב היום על התרומה האפשרית של המחקר הזה להבנת בריאות הנפש?
"לצערי עדיין לא השלמנו את המעגל. אנחנו עדיין חושבים שמחלות פסיכיאטריות נובעות ממשהו תקול בקשר בין התאים, ולפעמים החוויה היא זו ששינתה את הקשרים ביניהם, ואולי היא לא עשתה את זה טוב. חוקרים כבר מתחילים למצוא גנים שמתווכים את היכולת של חוויה בעייתית להשפיע על חוזק הסינפסה, כלומר התחום מתפתח יפה אבל עדיין אין לנו הסברים באמת טובים".
מה אתה חוקר כרגע?
"אני היום די בסוף הקריירה שלי, כך שאני לא עושה משהו חדש לגמרי. אני מנסה להשלים את הקטלוג של תאי הרשתית - הקשר בין הגנטיקה שלהם לפונקציה שלהם ולתאים האחרים שאליהם הם קשורים - וחוקר גם את האבולוציה שלהם. לכל בעלי החוליות יש רשתית יחסית דומה, בניגוד נניח לקליפת המוח (Cortex) שלצפרדעים לדוגמה אין בכלל. אבל למרות שלכל בעלי החיים יש תאים דומים ברשתית, מספר התאים מכל סוג הוא שונה מאוד והם כנראה משתמשים בהם אחרת. אנחנו מנסים להבין מהם הסוגים הדומיננטיים במשפחות החיות העיקריות.
"בעיניי זה קצת כמו להסתכל על אבולוציה גנטית. חוקרי אבולוציה אוהבים להסתכל על הגנים ולומר, 'הנה גן שמור בחיות רבות, אולי הוא עושה משהו מאוד חשוב ובסיסי, והנה גן שהופיע רק אצל המין הזה, אולי הוא עושה משהו מאוד ייחודי לאותו מין'. אותו דבר נכון גם לסוגי תאים. האם יש חלק של הרשתית שנשאר קבוע וחלק אחר שבו מתרחשת עיקר האבולוציה?".
ממוח על שבב ועד השתלת תאים: 3 טכנולוגיות חדשות בחקר המוח מעלות שאלות אתיות
ב-2021 כיהן סיינס כסגן יו"ר ועדה של ה-NIH (המכון הלאומי לרפואה בארה"ב) ושל האקדמיה הלאומית למדע, הנדסה ורפואה בארה"ב, שביקשה לבדוק את ההשלכות האתיות של שלוש טכנולוגיות מחקר חדשות: גידול צברי מוח זעירים במעבדה ("מוח על שבב"), השתלה של תאי מוח אנושיים בבעלי חיים והשתלה של תאי מוח מאדם אחד לאדם אחר.
"אם אני לוקח את הכליה שלי ואני שם אותה בתוכך, אני עדיין אני ואת עדיין את", אומר סיינס, "אבל כשמדובר במוח, אנחנו כבר לא כל כך בטוחים".
"אין לנו מושג איך נראית תודעה"
הטכנולוגיה המתקדמת ביותר היום בין אלה היא צבר תאי המוח על שבב. "זה כלי מחקר מאוד יעיל", אומר סיינס. "הוא מאפשר לראות את ההבדל בתקשורת בין תאי העצב אצל אנשים עם מחלה ואצל אנשים ללא מחלה. זה מחקר שאי אפשר לבצע במוח האנושי. היום צברי התאים האלה הם מאוד קטנים, לא מתפתחים מעצמם ולא מאוד מאורגנים. הם לא מאוד שונים מעובר בתחילת דרכו, ואין להם שום יכולת להתפתח בלי מקור מידע חיצוני. אין היום שום סיבה לחשוב שיש להם כאב או מודעות. אבל הטכנולוגיה הזאת מתפתחת מהר, ולכן אנחנו חייבים להיות עם היד על הדופק, ולהמשיך לבחון מה קורה כשהמורכבות עולה. מתי זה יקרה? אני לא יודע".
איך נדע שעברנו איזשהו רף לכיוון של משהו שהוא באמת דמוי מוח?
"אנחנו היום לא יודעים מה זו תודעה. אין לנו שום מושג איך תודעה נראית במוח, אז אנחנו כנראה לא נוכל לזהות אותה גם בצבר התאים. לכן אני מעריך שקודם כל נחפש את סימני הכאב. כיוון אחר יהיה לומר שאנחנו לא רוצים לעבור רמת מורכבות מסוימת, אפילו אם אין לנו הוכחה שמשמעותה אכן כאב או מודעות".
כמה זמן ייקח לנו להגיע לאזורים המסוכנים האלה? זה יקרה בימי חיינו?
"תלוי כמה זמן נחיה. אבל הטכנולוגיה מתקדמת כל כך מהר, שאני לא לגמרי שולל את האפשרות שזה יקרה בימי חיי".
"שוללים מהקוף את קופיותו"
שני התחומים האחרים מתפתחים לאט יותר.
"כן ולא. השתלה של תאי חיה במוח אדם, זה כיוון שנחקר כבר הרבה זמן. מדובר עדיין בכמות תאים קטנה, אבל החשש הוא שאם נשים כמות גדולה של תאי תורם בתוך המושתל כבר לא נדע במוח של מי מדובר. כבר היום אנחנו מגדלים חלקים של מוח של עכבר אחד בתוך עכבר שני, וזה מאוד יעיל להפריד בין גורמים סביבתיים ומולדים למחלות. אבל אי אפשר היום לעשות זאת עם תאים של בני אדם בעכבר, או של עכבר בבני אדם, מכל מיני סיבות שתלויות בתנאים השונים שנדרשים לכל אחד מסוגי התאים להתפתח, וזה לא צפוי להשתנות בשנים הבאות, להערכתי עוד עשורים.
"לגבי תאי אדם במוח של קוף ולהיפך, אני פחות נחרץ. יש עדיין חסמים טכנולוגיים, אבל המדע מתקדם מאוד מהר, ואפשר יהיה אולי ליצור עוד בימי חיינו קוף עם קליפת מוח של אדם. ואז השאלה היא - עבור מי הבעיה האתית גדולה יותר, האם עבור האדם או עבור הקוף? כשאני שואל אתיקאים, כולל אנשי דת מדתות שונות, מעניין שהם בדרך כלל רואים כאן בעיה אתית יותר גדולה עבור הקוף. אנחנו בעצם מוחקים את ה'קופיות' שלו".

עכבר מעבדה / צילום: Shutterstock
ומה לגבי השתלת תאים מאדם לאדם? תלוי איזה תאים. "נראה שאיש לא מוטרד מהשתלה של כמה נוירונים מפרישי דופמין באזור התנועה של חולה פרקינסון. זה אפילו נמצא בניסויים קליניים. אבל בשלב מסוים אולי נרצה להשתיל תאים שאחראים לפונקציות גבוהות יותר (פונקציות קוגניטיביות מורכבות כמו למידה, קבלת החלטות, רגשות - ג"ו). זה אולי יהיה מדאיג, אבל זה מאוד רחוק. אנחנו עדיין לא מבינים כמעט כלום לגבי הפעילות של המוח בהקשר של הפונקציות הגבוהות, אז לנסות להעביר פונקציות גבוהות מאדם לאדם, זה נראה מאוד רחוק".
למרות כל הבעיות האתיות הללו, סיינס מאמין שכדאי להתקדם בשלושת הכיוונים. "המחלות הכי גרועות ונפוצות בעולם קשורות בתאי מוח. אין הרבה התקדמות בחקר המחלות הללו, ואחת הסיבות לכך - יש על כך הסכמה רחבה - היא שמודל העכבר הוא לא טוב לחקר המחלות הללו. צריך למצוא פתרון אחר".
פרופ' ג'ושוע סיינס
אישי: בן 73, נשוי ואב לשניים. מתגורר במסצ'וסטס, ארה"ב. הספרים הרבים שהחזיקו הוריו בבית הציתו אצלו עניין בפסיכולוגיה, שהתפתח לעניין בביולוגיה של המוח
מקצועי: למד ביוכימיה ופסיכולוגיה בייל, והמשיך לדוקטורט בנוירוביולוגיה בהרווארד. אחרי 24 שנה כחוקר באונ' וושינגטון, גויס להקמת המרכז לחקר המוח בהרווארד
עוד משהו: כבר בתיכון עבד במעבדה שחקרה את הקשר בין מחלות נפש לזיהום חיידקי